25 октября президиумом Совета при Президенте РФ по стратегическому развитию и приоритетным проектам утвержден паспорт приоритетного проекта "Внедрение автоматизированной системы мониторинга движения лекарственных препаратов от производителя до конечного потребителя для защиты населения от фальсифицированных лекарственных препаратов и оперативного выведения из оборота контрафактных и недоброкачественных препаратов". Его краткое наименование — "Лекарства. Качество и безопасность".

Отметим, что Российская Федерация не первая страна мира, в которой внедряется маркировка лекарственных средств. Европейская директива о маркировке (Directive 2001/83/EC) начала работать во Франции с 2011 года, но обязательной она станет с этого года. В США программа сериализации (the Drug Supply Chain Security Act) работает с 2015 года, но только на уровне серий, а на уровне отслеживания отдельных пачек — с конца текущего года. Маркируют лекарственные препараты в Турции, Объединенных Арабских Эмиратах.
Система мониторинга лекарственных препаратов в России будет внедряться с 1 января 2020 года одномоментно по всей стране. По официальным оценкам, при полном охвате лекарственных препаратов система будет отслеживать свыше 6.5 млрд. упаковок ежегодно, до одной тысячи производителей, до 2,5 тыс. оптовых организаций (в РСО-А – 22), до 350.000 медицинских организаций и пунктов выдачи аптек (в РСО-А – более 700). А всё население РФ получит возможность проверить легальность приобретаемых лекарств с помощью мобильного приложения или общедоступного сканера. К слову, уже сейчас для свободного скачивания доступны приложения для смартфонов "Проверка маркировки товаров", позволяющие путем сканирования QR-кода получить информацию о происхождении упаковки лекарства и убедиться, что препарат легален.
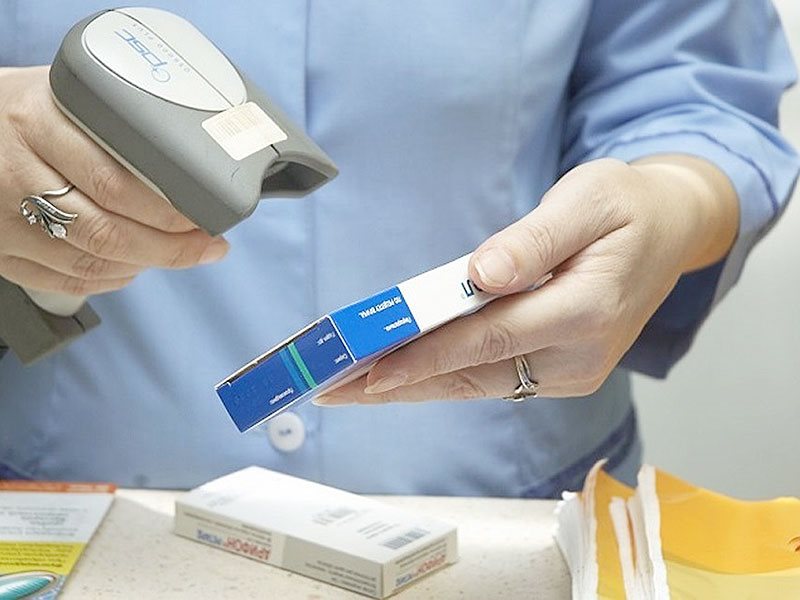
По такому же принципу, только с использованием специализированных приборов, сканеров, предполагается проводить проверку подлинности лекарственных средств в аптеках и медицинских учреждениях при получении их от поставщика. Таким образом, все аптечные и медицинские организации должны пройти регистрацию в системе "Маркировка" и закупить необходимое оборудование для сканирования лекарственных препаратов.
О том, как обстоят дела в этой сфере в Северной Осетии, рассказала "СО" руководитель Росздравнадзора по РСО-А Ольга ДАВЫДОВА.
– В течение всего 2019 года осуществлялось подключение к системе "Маркировка" медицинских и аптечных организаций нашей республики. Приказом министерства здравоохранения созданы центры компетенции, которые определены в качестве обучающих центров на региональном уровне и оказывают методическую помощь другим участникам фармацевтического рынка республики. Функционируют данные центры на базе АО "Фармация" – для аптечных организаций и Республиканской клинической больницы МЗ РСО–А – для медицинских. На территории нашей республики вся деятельность по осуществлению внедрения маркировки лекарственных средств курируется непосредственно заместителем председателя Правительства РСО–А, министром здравоохранения Т.К. Гогичаевым, при непосредственном участии Территориального органа Росздравнадзора по Северной Осетии.
По состоянию на 18.10.2019 года, в федеральной информационной системе "Маркировка" зарегистрированы 260 из 750 участников от РСО–А (35%), в том числе, в 100% случаев зарегистрированы медицинские организации, подведомственные минздраву республики. И тем не менее этого недостаточно и свидетельствует о низкой активности субъектов обращения лекарственных средств в данном вопросе. Руководителям профильных организаций республики следует отнестись к вопросу серьезнее и принять исчерпывающие меры для решения всех проблем, связанных с внедрением системы маркировки лекарственных средств.
Под маркировкой понимается информационная запись, которая в виде штрих-кода наносится на первичную и вторичную лекарственную упаковку. Уникальность его значений позволяет идентифицировать товар и узнать о его «судьбе» с момента производства.
"Цель проекта: защита населения от фальсифицированных, недоброкачественных и контрафактных лекарств и предоставление потребителям возможности проверки легальности препаратов, находящихся в гражданском обороте, обеспечение прозрачности и справедливой конкуренции на фармацевтическом рынке"
Обращаем внимание, что юридические лица и индивидуальные предприниматели, осуществляющие производство, хранение, ввоз в Российскую Федерацию, отпуск, реализацию, передачу, применение и уничтожение лекарственных препаратов для медицинского применения, должны обеспечить внесение информации о них в систему мониторинга с 1 января 2020 года. За производство или продажу лекарств без нанесения средств идентификации, с нарушением установленного порядка их нанесения, а также за несвоевременное внесение данных в систему мониторинга юрлица и ИП несут ответственность в соответствии с законодательством РФ. Соответствующие изменения уже внесены в Кодекс об административных правонарушениях РФ. Так, с 1 января 2020 года вступают в силу изменения в Кодекс РФ об административных правонарушениях (ФЗ № 58-фз от 15.04.2019 г.), которые дополнили главу 6 статьей 6.34. Административные нарушения, предусмотренные данной статьей, влекут наложение административного штрафа на должностных лиц в размере от 5 до 10 тысяч рублей; на юридических лиц (в том числе индивидуальных предпринимателей) – от 50 до 100 тысяч рублей!
С 1 октября 2019 года на территории Российской Федерации уже введена обязательная маркировка лекарственных препаратов семи высокозатратных нозологий (7 ВЗН). В нашей стране зарегистрировано и разрешено к медицинскому применению 27 международных непатентованных наименований лекарственных препаратов перечня семи высокозатратных нозологий.
К обязательной маркировке лекарственных препаратов 7 ВЗН готово и Акционерное общество "Фармация", которое осуществляет отпуск данной категории препаратов через 14 своих аптечных организаций. Все аптеки оборудованы необходимыми сканирующими устройствами.
Вместе с тем уже можно подвести предварительные итоги. Так, в России внедрение маркировки лекарств за время проведения эксперимента (с февраля 2017 года) позволила снизить объем недоброкачественной продукции на рынке в 2,5 раза. Об этом на парламентских слушаниях в Государственной думе РФ рассказал глава Росздравнадзора Михаил Мурашко.
-
 Зажженный вами не погаснет свет!05.10.2018 14:45
Зажженный вами не погаснет свет!05.10.2018 14:45 Редакция01.01.2017 8:00
Редакция01.01.2017 8:00 -
 Реклама и реквизиты01.01.2017 2:30
Реклама и реквизиты01.01.2017 2:30 Упрощенная бухгалтерская (финансовая) отчетность01.05.2016 17:45
Упрощенная бухгалтерская (финансовая) отчетность01.05.2016 17:45 -
 Разжижаем кровь13.06.2018 16:45
Разжижаем кровь13.06.2018 16:45 Фокус фикуса Бенджамина27.09.2024 15:25
Фокус фикуса Бенджамина27.09.2024 15:25 -
 ОрджВОКУ - 100 лет!20.11.2018 12:15
ОрджВОКУ - 100 лет!20.11.2018 12:15 150-летие технологическому колледж полиграфии и дизайна, 15 октября 201830.10.2018 15:30
150-летие технологическому колледж полиграфии и дизайна, 15 октября 201830.10.2018 15:30